[서울=뉴스핌] 정경환 기자 = 식품의약품안전처는 전 세계적으로 코로나19 치료제 및 백신 개발이 활발히 진행되고 있는 가운데, 현재 국내에서 진행 중인 코로나19 치료제 및 백신 임상시험은 총 21건이라고 10일 밝혔다. 치료제가 19건, 백신이 2건이다.
먼저, 치료제로는 항바이러스제와 중화항체치료제, 혈장분획치료제, 면역조절제가 개발 중이다. 부광약품(레보비르, 항바이러스제), 엔지켐(EC-18, 면역조절제), 신풍제약(피라맥스, 항바이러스제), 대웅제약(DWJ1248, 항바이러스제), 셀트리온(CT-P59, 중화항체치료제), 녹십자(GC5131, 혈장분획치료제) 등이 환자를 모집해 임상을 진행하고 있다.
백신은 제넥신(GX-19)이 환자를 모집해 임상을 진행 중이다.
또한, 대체치료수단이 없는 환자에 치료기회 제공을 위해 녹십자 혈장분획치료제의 치료목적사용이 3건 승인됐다. '임상시험의약품 치료목적사용'은 생명이 위급하거나 대체치료수단이 없는 응급환자 등의 치료를 위해 임상시험용의약품을 식약처 승인을 받아 사용하는 제도다.
식약처 측은 "코로나19 치료제·백신의 국내외 개발 동향을 지속적으로 모니터링하고 있다"며 "현재 개발 속도가 빠른 분야는 '항체치료제'다"라고 언급했다.
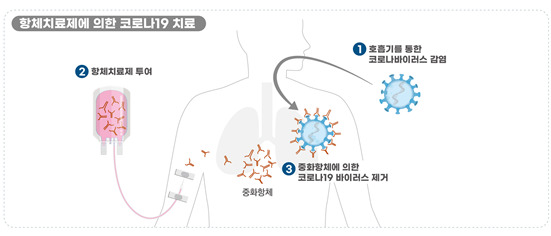
항체치료제는 코로나19 완치자의 혈액에서 강력한 바이러스 중화능력을 보이는 항체를 선별하고, 그 항체 유전자를 삽입한 세포를 배양해 대량 생산된 항체로 만든 의약품을 말한다.
국내에서 개발되고 있는 항체치료제로 셀트리온이 코로나19 경증~중등증 환자를 대상으로 2/3상 임상을 다국가 임상으로 진행하고 있다.
해외에서 개발되고 있는 항체치료제로는 미국의 릴리와 리제네론의 제품이 코로나19 경증~중등증 환자를 대상으로 2/3상 임상시험을 진행 중이다.
두 제품 모두 미국 식품의약국(FDA)에 지난달 7일 긴급사용승인을 신청했으며, 이 중 릴리의 제품이 지난 9일 승인을 받았다.
릴리에서 진행 중인 2상 임상의 중간결과 발표(10월 28일)에 따르면, 대조군 대비 시험군에서 증상 악화로 입원하는 비율이 감소했으며, 안전성 우려는 없는 것으로 나타났다. 다만, 별개로 진행 중인 중증환자 대상 3상 임상은 치료 효과가 부족한 것으로 나타나 조기에 종료(10월 26일)됐다.
리제네론에서 진행 중이던 중증환자 대상 3상 임상은 독립적 데이터 모니터링 위원회의 권고에 따라 추가적인 안전성 평가를 위해 지난달 30일 증상이 심각한 중증환자에 대한 등록을 중단했다.
독립적 데이터 모니터링 위원회 임상 대상자에 대한 안전성을 확보하고 임상의 효과와 안전성을 평가하는 등 전반적인 시험 수행을 모니터링하는 위원회로, 임상을 계속 진행할 것인지 또는 중지할 것인지에 대해 권고한다.
한편, 국내에서 승인한 임상시험은 현재 총 28건(치료제 26건, 백신 2건)이다.
코로나19 치료제에 대한 임상시험 2건이 지난 10월 27일 이후 추가로 신규 승인되고, 7건이 종료돼 현재 진행 중인 임상은 총 21건(치료제 19건, 백신 2건)이다.
신규 승인된 임상은 한국엠에스디(MK-4482, 항바이러스제)의 2/3상(10월 29일 승인)과 뉴젠테라퓨틱스(뉴젠나파모스타트정, 항바이러스제)의 1상(11월 3일 승인)이다.
한국엠에스디의 'MK-4482'는 독감 치료제로 개발 중인 신약을 코로나19 치료제로 개발하는 것으로 다국가 임상으로 진행되고 있다.
뉴젠테라퓨틱스의 '나파모스타트'는 현재 항응고제로 사용되는 주사제(나파모스타트메실산염)를 경구 투여할 수 있는 정제로 개발해 복용 편의성을 개선한 제품이다.
제약업체가 진행하고 있는 임상은 18건이며, 연구자가 진행하고 있는 임상은 3건이다.
제약업체가 진행하는 임상은 ▲1상 임상 7건(항체치료제, DNA백신 등) ▲2상 임상 9건(혈장분획치료제 등) ▲3상 임상 2건이다.
식약처 측은 "코로나19 치료제·백신의 임상승인, 품목허가, 특례제조·수입 등에 대한 사항을 지원해 우리 국민이 치료 기회를 보장받을 수 있도록 최선을 다하겠다"고 했다.
hoan@newspim.com























