[서울=뉴스핌] 이나영 기자= 앱클론이 상하이 헨리우스 바이오텍(헨리우스)에 기술이전(L/O)해 HER2 양성 위암환자 대상 1차 치료제로 임상2상이 진행 중인 AC101(헨리우스 코드명: HLX22)에 대해, 헨리우스가 미국임상종양학회(ASCO) 소화기암 심포지엄인 ASCO GI(샌프란시스코)에서 18일(현지시간) 전체 53명의 환자를 대상으로 한 임상2상 중간결과를 발표했다고 밝혔다.
위암은 매년 약 100만명의 새로운 환자가 발생하고 있으며, 발병률이 전 세계 암 발생 중 5번째를 기록하고 있는 매우 위협적인 질환이다. 특히 진행형 위암의 경우 5년간 환자 생존율이 6%밖에 되지 않는다. 이 중 HER2 양성 비율은 위 또는 위-식도 접합부 선암의 20% 내외에서 관찰되고 있으며, 치료 예후도 좋지 않은 것으로 알려져 있다. 그럼에도 불구하고 ADC(항체-약물 결합체)를 비롯해 기존의 어떠한 치료제로도 충분한 효과를 보이지 못해 새로운 치료법 개발이 절실한 상황이다.
이날 발표된 AC101(HLX22)의 임상2상 중간결과 내용에 따르면, HER2 양성 국소 진행성·전이성 환자를 대상으로 현재 사용되는 표준 치료제 HLX02(허셉틴 바이오시밀러)+XELOX 투여 요법보다 AC101까지 병용투여했을 때 더욱 뛰어난 치료 효능을 보였다.
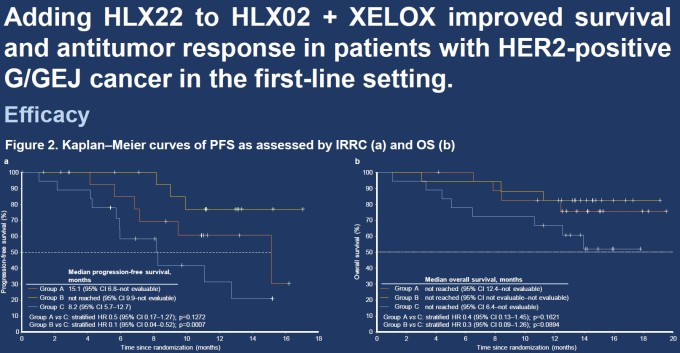
이번 임상은 AC101 저용량 병용투여군(15mg/kg), AC101 고용량 병용투여군(25mg/kg), 비교 대조군 등 3개 군으로 나뉘어 진행됐다. 투여 후 48주에 측정된 객관적 반응율(ORR)은 저용량군에서 58.8%, 고용량군에서 38.9%, 비교 대조군에서 16.7%로 나타났으며, 특히 저용량군에서 비교 대조군보다 치료 효과가 3배 이상 우수한 것이 관찰됐다.
무진행 생존기간(PFS)의 중간값은 비교 대조군에서 8.2개월을 보인 반면 고용량군에서 15.1개월을 보였으며, 저용량군에서는 아직까지 중간값에 도달하지 않은 것으로 분석돼 우수성이 확인됐다.
전체생존율은 임상이 진행 중이어서 모든 군에서 중간값에 도달하지 않았으나, 고용량군과 저용량군에서 전체생존율의 위험율이 비교 대조군 보다 낮은 것으로 발표됐다. 또한 약물 치료 후 종양이 다시 커지기 전까지 반응이 지속되는 기간인 종양반응기간(DOR)도 비교 대조군에서 6.8개월, 고용량군에서 12.4개월, 저용량군에는 중간값에 도달하지 않아 AC101 병용투여의 뛰어난 효능을 보여주었다.
회사 관계자는 "당사에서 개발한 AC101은 HER2를 대상으로 하는 위암 항체치료제로서, 허셉틴 항체와 병용 시 효과가 더욱 뛰어나 HER2 양성 위암에서의 1차 표준치료제로서의 가능성을 확고히 보여 주고 있다"면서 "특히 헨리우스는 자사가 개발한 허셉틴 바이오시밀러와 AC101의 병용요법을 통해 치료효과를 극대화하는 것은 물론, 시장에서도 높은 경쟁력을 확보할 수 있을 것으로 기대하고 있다"고 전했다.
한편, 앱클론은 AC101의 중국 임상 및 글로벌 임상의 진행 단계에 따른 마일스톤, 상업화 시 매출에 대한 로열티를 수령하게 된다.
nylee54@newspim.com























