MMR 결핍 세포에서의 TMZ 민감성 향상
[세종=뉴스핌] 이경태 기자 = 울산과학기술원(UNIST)과 기초과학연구원(IBS) 연구진이 교모세포종의 항암제 내성을 극복할 단서를 19일 발표했다. 교모세포종은 환자의 90%가 5년 내 사망하는 악성 뇌종양으로, 현재 치료 가능한 항암제는 테모졸로마이드(TMZ) 단 하나다.
안톤 가트너 교수팀(UNIST)과 이세민 교수팀(바이오메디컬공학), IBS 유전체항상연구단은 APE1이 교모세포종의 항암제 저항성에 중요한 표적 유전자라는 연구 결과를 도출했다. 이 표적 유전자를 억제하는 약물을 TMZ와 병용하면 치료 효과를 증대할 것으로 기대되고 있다.
TMZ는 세포 DNA를 손상시키는 방식으로 항암 작용을 하지만, 암세포는 이를 복구하여 치료가 어렵다. 연구팀은 19개의 DNA 복구 경로에 관여하는 47개 단백질 유전자를 불활성화한 세포주를 제작한 후, TMZ에 대한 민감성을 평가했다.
실험 결과, APE1 단백질 발현을 억제하면 MMR 유전자가 결핍된 TMZ 내성 세포에서도 항암제에 대한 민감성이 향상됐다. MMR 유전자 결핍은 TMZ 내성의 원인 중 하나로 알려져 있다.
반면 MPG 단백질 발현 억제는 항암제 민감성에 영향이 없었다. MPG와 APE1 단백질 모두 BER(기초 복구) 경로에 참여하지만 서로 다른 효과를 발휘했다.
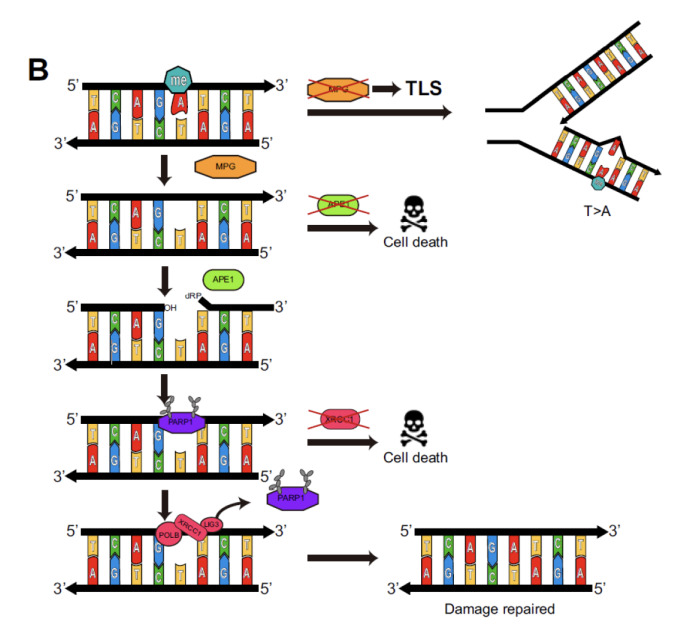
단백질 발현 억제가 항암제 내성 개선에 미치지 않은 이유는 세포가 TLS(대체 복구 경로)를 활용하기 때문으로 분석됐다. 연구팀은 TLS 경로와 관련된 단백질 유전자도 항암제 내성 억제의 표적이 될 수 있다는 것을 밝혔다.
이번 연구는 항암제 내성과 노화 간의 관계도 밝혀냈다. 노화로 축적된 DNA 돌연변이 패턴이 TMZ 대응 과정에서 세포에 축적된 패턴과 유사한 것으로 나타났다. 이는 TLS 중합 효소 제타가 노화 및 TMZ 내성 세포에서 돌연변이를 유도하는 것을 시사한다.
biggerthanseoul@newspim.com

















