재고관리·부작용 등 부담도…미국서도 백신 임상 치료제의 4% 수준
[서울=뉴스핌] 박다영 기자 = 코로나19와 관련해 국내에서 10건이 넘는 임상시험이 진행 중인 치료제와 달리 백신은 단 두 건에 그쳐 그 배경에 관심이 모아진다. 코로나19 치료제·백신 개발을 끝까지 지원하겠다는 정부 의지에도 불구, 백신은 치료제와 달리 공공성이 커 제약·바이오 기업들이 수익모델을 만들어내기가 어렵기 때문이라는 분석이 나온다.
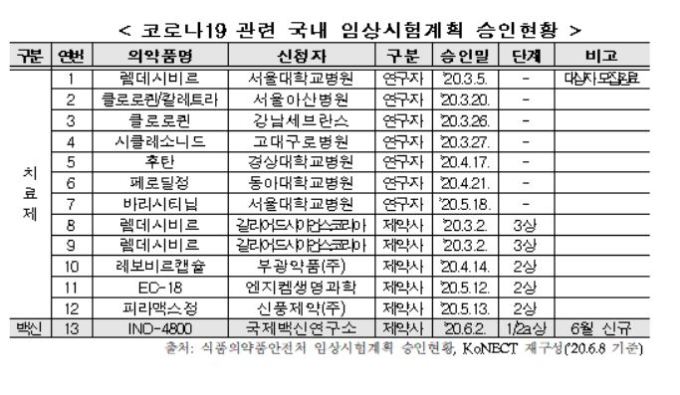
12일 관련 업계와 국가임상지원재단에 따르면 현재 진행 중인 코로나19 백신 임상시험은 2건에 불과하다.
국제백신연구소가 신청한 미국 바이오기업 이노비오의 후보물질 'INO-4800'과 제넥신의 DNA 백신 'GX-19' 다.
반면, 코로나19 치료제 임상시험은 12건에 이른다. 길리어드사이언스코리아의 에볼라 치료제 '렘데시비르'를 비롯해 부광약품, 엔지켐생명과학, 신풍제약 등 12건의 임상시험이 순항 중이다.
치료제는 바이러스에 감염된 환자에게 투여해 바이러스의 복제를 막는다. 이와 달리 백신은 감염되기 전 미리 투여해 체내에서 항체를 생성하고 스스로 바이러스에 저항하도록 하는 예방기능의 의약품이다.
응급 환자나 중증 환자의 치료 목적이 아니라, 예방을 위해 맞는 백신은 공공재 성격이 강하다. 현재 기본 백신은 정부 또는 국제기구가 입찰 방식으로 구매하고 있어 정부의 가격 통제가 심하다. 개발 업체 입장에서 비용 대비 효용성을 따졌을 때 치료제에 비해 수익성과 시장성이 떨어지는 것이다.
재고 관리의 문제도 있다. 독감 백신의 경우 그 해 소진되지 못한 재고는 전부 폐기한다. 코로나19처럼 전파력이 강한 감염병은 사전에 필요한 백신 물량을 예측하기가 어렵다.
업계 관계자는 "백신은 제약·바이오 기업이 보관이 어려운 데다가 수익모델을 찾기가 어려워 접근이 잘 안 된다"며 "공공 생산시설이나 대규모 자금 지원이 있지 않다면 개별 기업이 치료제 대신 백신 개발을 선택하기는 어려울 것으로 보인다"라고 말했다.
더불어 코로나19 바이러스는 리보핵산(RNA)으로 이뤄져 변이가 잘 일어나기 때문에 개발이 어렵다. RNA 바이러스 중 백신이 있는 것은 독감인데, RNA의 변이로 독감 백신은 매년 새로 만드는 실정이다.
현재 국내에서 개발 중인 코로나19 백신은 합성항원 백신과 핵산(DNA) 백신 등 두 가지다. 합성항원 백신은 코로나19 바이러스의 단백질 일부를 선별해 유전자 재조합기술로 합성해 만든다. 국내 기업 가운데 SK바이오사이언스와 HK이노엔이 이 백신을 개발하고 있다.
DNA 백신은 바이러스가 아닌 DNA 일부를 인체에 주입해 면역반응을 유도한다. 이노비오, 제넥신 컨소시엄, 진원생명과학이 개발 중인 백신이 여기에 해당한다.
미국 바이오기업 모더나가 개발하고 있는 백신도 핵산백신의 한 종류로, DNA 대신 mRNA를 주입한다.
마지막으로 백신은 부작용에 대한 부담이 치료제에 비해 상대적으로 크다. 백신은 면역력을 갖기 위해 약한 병균독소를 인체에 주입한다. 드물게 열이 나거나 입원치료가 필요하다. 심한 경우에는 사망까지 이르기도 한다. 환자만 복용하는 치료제보다 전국민이 맞는 백신의 부작용에 대한 리스크는 클 수밖에 없다.
이 같은 어려움 때문에 국내뿐 아니라 해외에서도 백신 관련 임상시험은 치료제에 한참 못 미친다. 미국국립보건원(NIH)의 임상정보 제공 사이트 클리니컬트라이얼에 등록된 코로나19 치료제 임상시험은 지난 8일 기준 825건인 반면, 백신은 33건에 그쳤다. 치료제 임상의 4% 수준이다.
업계 관계자는 "코로나19는 일반 백신보다 더 개발이 어려운 데다가 가격, 재고, 부작용 등을 따졌을 때 기업이 리스크를 안기가 쉽지 않을 것으로 생각된다"고 말했다.
allzero@newspim.com























