알츠하이머 등 퇴행성 질환 연구 기여
[세종=뉴스핌] 이경태 기자 = 희귀 유전성 질환인 헌팅턴병의 원인 단백질이 신경세포의 구조적 뼈대를 물리적으로 조직하는 핵심 기능을 수행한다는 사실이 국내외 공동연구진에 의해 세계 최초로 밝혀져, 헌팅턴병뿐 아니라 알츠하이머병, 파킨슨병 등 다른 퇴행성 질환 연구에도 새로운 돌파구가 마련될 전망이다.
한국과학기술원(KAIST)은 생명과학과 송지준 교수 연구팀이 오스트리아 과학기술원(ISTA), 프랑스 소르본느대/파리 뇌연구원, 스위스 연방공대(EPFL)와의 국제 공동연구를 통해 초저온 전자현미경과 세포생물학적 기법으로 헌팅틴 단백질이 세포골격 미세섬유를 다발 형태로 배열하는 구조적 원리를 규명했다고 1일 밝혔다.
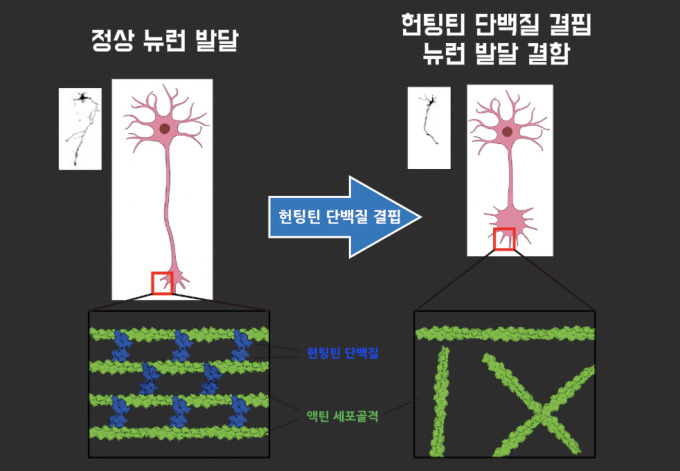
연구팀에 따르면 헌팅틴 단백질은 세포골격 미세섬유에 직접 결합하며, 두 개의 헌팅틴 단백질이 짝을 이루면서 약 20나노미터 간격으로 세포골격을 가지런히 묶어준다. 이렇게 형성된 세포골격 다발은 신경세포 간 연결망 발달에 핵심적 역할을 하는 것으로 확인됐다.
그동안 헌팅틴 단백질은 소포 운반이나 미세소관 기반 수송에 관여하는 등 세포골격을 '쓰는' 역할만 한다고 알려져 있었다. 이번 연구는 헌팅틴 단백질이 세포골격 자체를 물리적으로 조직한다는 사실을 분자 수준에서 처음으로 증명해 학계의 주목을 받고 있다.
헌팅턴병은 근육 조정 능력 상실, 인지 기능 저하, 정신적 문제를 동반하는 대표적인 신경계 퇴행성 질환이다. 전 NBC 뉴스 기자 찰스 서빈과 미국의 전설적 포크 가수 우디 거스리가 이 병을 앓은 것으로 알려져 있다. 연구팀 실험 결과 헌팅틴 단백질이 결핍된 신경세포에서는 신경세포의 구조적 발달이 저해되는 현상이 실제로 관찰됐다.
제1저자인 KAIST 김재성 박사과정생은 "그동안 베일에 싸여 있던 불치병인 헌팅턴병 원인 단백질의 작용 기전을 이해하는 새로운 관점을 제시했다"고 말했다.
송지준 교수는 "이번 성과는 헌팅턴병 발병 메커니즘을 이해하는 데 중요한 단서를 제공할 뿐 아니라, 세포골격 관련 질환 연구에도 파급 효과가 클 것으로 기대한다"며 "세포 분열, 이동, 기계적 신호 전달 등 다양한 생명 현상에서 헌팅틴 단백질의 역할을 새롭게 조명할 수 있는 길을 열었다"고 밝혔다.
이번 연구는 KAIST 김재성 박사과정생·김형주 박사(현 하버드대), 파리 뇌연구원 헤미 카펜티어 연구원, 마리아 크리스티나 가피치 연구원 등이 제1 저자로 참여했으며, 국제 학술지 '사이언스 어드밴시스' 지난달 19일 자에 게재됐다. 연구는 보건복지부 글로벌연구협력지원사업 및 한-오스트리아 협력기반조성사업의 지원을 받아 수행됐다.
biggerthanseoul@newspim.com























