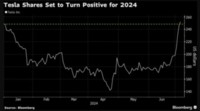
유럽의약품청 산하 위원회, 허가 권고…2개월 낸 최종 승인 예상
[뉴스핌=한태희 기자] SK케미칼이 내놓은 혈우병 치료제가 유럽에서 시판 허가를 앞두고 있다.
SK케미칼은 혈우병 치료제 '앱스틸라(AFSTYLA)'가 유럽의약품청(EMA) 산하 인체약품위원회로부터 시판 허가를 권고 받았다고 15일 밝혔다.
보통 EMA 인체약품위원회가 허가 권고를 결정하면 1~2개월 안에 최종 승인이 떨어진다. 이에 따라 빠르면 올 연말이나 늦어도 내년 초에 앱스트라 시판 허가가 날 전망이다.
이에 앞선 지난 5월 SK케미칼은 미국 식품의약국(FDA)으로부터 시판 허가를 받았다. 현재 미국에서 앱스틸라를 판매 중이다. 또 EU(유럽연합) 외에도 스위스와 호주에서 허가 심사 단계에 있다.
 |
| <사진=SK케미칼> |
SK케미칼은 자체 기술로 앱스틸라를 개발했다. 지난 2009년 글로벌 바이오의약품 기업인 CSL에 기술 이전하며 라이센스 아웃을 했다. CSL이 생산 공정개발과 글로벌 임상 및 허가 신청을 맡았다.
앱스틸라는 '생체 안에서 결합력이 높아 안정적이고 약효가 지속되는 혈우병 치료제'란 뜻을 담고 있다. SK케미칼은 A형 혈우병 치료에 공을 들였다. A형 혈우병은 혈액 응고에 관여하는 13가지 인자 중 8번째 인자가 부족하면 발생한다. 이에 SK케미칼은 '단일 사슬형 분자구조'를 가진 제8인자를 앱스틸라에 접목했다. 기존 치료제는 분리된 단백질 두개가 연합된 모양이다. 반면 앱스틸라는 두 단백질을 하나로 결합시킨 형태다.
임상 결과 부작용 또한 없었다. A형 혈우병 치료제 부작용으로 알려진 약물 효과를 저해하는 항체가 생기는 현상이 단 한건도 보고되지 않았다는 게 SK케미칼의 설명이다.
한편 A형 혈우병 치료제 시장은 계속 커지고 있다. 글로벌리서치업체 데이터모니터에 따르면 전세계 A형 혈우병 치료제 시장은 오는 2020년 83억5000만달러(약 9조7803억원)까지 성장한다. 지난해 기준 시장 규모는 72억1000만달러(8조4450억원)다. 5년새 약 17% 증가할 전망이다.
[뉴스핌 Newspim] 한태희 기자 (ace@newspim.com)
 영상
영상