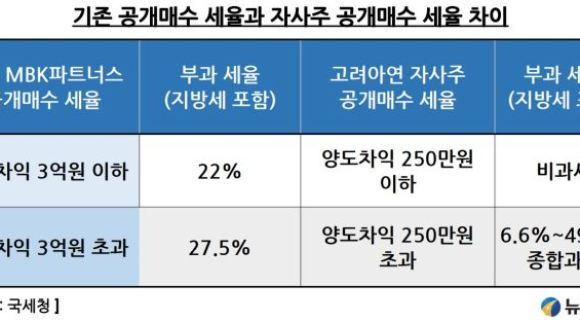
[서울=뉴스핌] 배요한 기자 = 제테마가 중국 국가약품감독관리국(NMPA)으로부터 보툴리눔 톡신 제테마더톡신주100U(JTM201, 수출용)에 대한 1/2상 임상시험계획(IND)을 승인 받았다. 지난해 10월 IND를 제출했던 제테마는 3개월만에 임상 승인을 받으면서, 계획했던 2026년 중국 시장 진출은 차질없이 진행될 전망이다.
6일 금융감독원 전자공시시스템에 따르면 제테마는 지난4일 중국 NMPA로부터 제테마더톡신주100단위 임상 1/2상 시험계획을 승인받았다고 밝혔다.
보툴리눔 톡신은 움직이는 표정근육의 움직임을 억제해서 주름을 치료하는 제제다. 제테마는 유럽소재의 국립기관으로부터 확보한 균주를 이용해 고순도 보툴리눔 독소를 생산하는 자체 기술을 개발을 완료했다. 지난 2020년 6월에는 식품의약품안전처(이하 식약처)로부터 제테마더톡신주 100U 수출용에 한해 품목허가를 받았다.
다만 최근 식약처가 국가출하승인 및 제조판매품목허가를 받지 않은 의약품 제조 및 판매를 이유로 제테마더톡신주100U의 품목허가를 취소하면서 글로벌 임상이 차질을 빚는 것 아니냐는 우려가 나오기도 했다. 지난달 식약처는 제테마더톡신주100U(수출용) 품목에 대해 품목허가 취소와 6개월간 제조업무정치 처분을 내렸다. 이에 제테마는 서울행정법원에 취소소송 및 집행정지를 신청했고, 법원으로부터 인용 결정을 받으면서 문제는 일시적으로 봉합된 상황이다.
 |
| 제테마 보툴리눔 톡신[사진=제테마] |
제테마 관계자는 "NMPA의 엄격한 허가시스템에도 불구하고 IND 승인이 빠르게 난 것으로 내부적으로 판단하고 있다"며 "최근 발생한 국내 식약처 관련 이슈는 영향이 없었던 것으로 본다"고 말했다.
이어 "향후 제테마더톡신은 중국인을 대상으로 미간주름 개선에 대한 안전성 및 유효성 평가를 위한 임상 1상과 2상 연구를 동시에 진행하게 된다"며 "연구시작 후 피험자 등록부터 데이터 분석 완료까지의 예상시간 약 15개월이 걸릴 것으로 예상된다"고 전했다.
지난해 2월 제테마는 중국의 화동 메디컬 에스테틱 바이오테크놀로지(HUADONG MEDICAL AESTHETICS BIOTECHNOLOGY)와 4억5900만 달러(한화 5827억원) 규모의 제테마더톡신의 독점 판매 계약을 체결했다. 제테마는 350만 달러(약 44억원)를 계약금으로 수령했고, 향후 임상진행단계에 따라 마일스톤으로 1250만 달러(약 158억원)를 받게된다. 독점판매 계약은 제품등록 시점부터 판매지역에 10년간 공급될 예정이다.
회사 관계자는 "이번 IND 승인이 빠르게 이뤄진 것은 중국 파트너사의 우수한 역량을 입증한 것"이라며 "임상 진행이 순조롭게 진행될 수 있도록 파트너사와 긴밀하게 협력해 나아갈 계획"이라고 전했다.
제테마더톡신은 국내에서 임상 3상을 진행 중이다. 회사 측은 빠르면 1분기, 늦어도 상반기 안에는 임상 3상 승인을 받을 것으로 기대하고 있다.
위해주 한국투자증권 연구원은 "제테마더톡신 국내 3상은 올해 상반기 종료되고, 2024년 1분기 내에는 품목허가를 받을 것으로 예상된다"며 "국내 임상 결과를 바탕으로 브라질, 호주, 뉴질랜드에서도 품목허가가 가능할 것"이라고 설명했다.
제테마는 중국 이외에도 브라질(1억2129만 달러)과 호주·뉴질랜드(1663만 달러) 지역의 현지 기업과 톡신 공급계약을 체결하며, 약 7000억원에 달하는 톡신 수출 계약을 성사시켰다.
yohan@newspim.com
 영상
영상